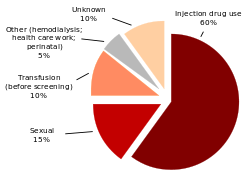Hepatitis C adalah infeksi yang terutama menyerang organ hati. Penyakit ini disebabkan oleh virus hepatitis C (HCV).
[1]
Hepatitis C seringkali tidak memberikan gejala, namun infeksi kronis
dapat menyebabkan parut (eskar) pada hati, dan setelah menahun
menyebabkan sirosis. Dalam beberapa kasus, orang yang mengalami sirosis
juga mengalami gagal hati, kanker hati, atau pembuluh yang sangat
membengkak di esofagus dan lambung, yang dapat mengakibatkan perdarahan
hingga kematian.
[1]
Seseorang terutama terkena hepatitis C melalui kontak darah,
penggunaan narkoba suntik, peralatan medis yang tidak steril, dan
transfusi darah. Sekira 130–170 juta orang di dunia menderita hepatitis
C. Para ilmuwan mulai meneliti HCV pada tahun 1970-an, dan memastikan
keberadaan virus tersebut pada tahun 1989.
[2] Virus ini tidak diketahui menyebabkan penyakit pada hewan lain.
Peginterferon dan ribavirin merupakan obat-obatan standar untuk HCV.
Antara 50-80% pasien yang diobati sembuh. Pasien dengan sirosis atau
kanker hati mungkin memerlukan transplantasi hati, namun biasanya virus
muncul kembali setelah transplantasi.
[3] Tidak ada vaksin untuk hepatitis C.
Gejala dan Tanda
Hepatitis C menunjukkan gejala akut hanya pada 15% kasus.
[4]
Gejalanya seringkali ringan dan tidak kentara, termasuk penurunan nafsu
makan, sakit kepala, letih, nyeri otot atau nyeri sendi, dan menurunnya
berat badan.
[5] Hanya sedikit kasus infeksi akut yang terkait dengan ikterus.
[6]
Infeksi ini dapat sembuh sendiri tanpa diobati pada 10-50% penderita,
dan lebih sering menyerang perempuan usia muda dibandingkan dengan
kelompok lain.
[6]
Infeksi kronis
Delapan puluh persen penderita yang terpajan virus hepatitis C akan mengalami infeksi kronis.
[7]
Sebagian besar pengalaman menunjukkan gejala minimal atau bahkan tidak
menunjukkan gejala sama sekali selama sepuluh tahun pertama infeksi,
[8] meskipun hepatitis C kronis dapat ditandai dengan kelelahan.
[9] Hepatitis C menyebabkan sirosis dan kanker hati pada orang yang telah terinfeksi selama bertahun-tahun.
[3]Sekitar 10–30% orang yang terinfeksi selama lebih dari 30 tahun akan mengalami sirosis.
[3][5] Sirosis lebih banyak terjadi pada orang yang juga terinfeksi hepatitis B atau HIV, pecandu alkohol, dan pada laki-laki.
[5] Orang yang mulai terkena sirosis memiliki risiko dua puluh kali lebih besar terkena kanker hati, sebanyak 1-3% per tahun.
[3][5] Pada pecandu alkohol, risiko ini menjadi 100 kali lebih besar.
[10] Hepatitis C merupakan penyebab utama pada 27% kasus sirosis dan 25% kasus kanker hati.
[11]
Sirosis hati dapat menyebabkan tekanan darah yang tinggi pada vena
yang mengalir ke hati, akumulasi cairan di perut, mudah memar atau
berdarah, vena melebar, khususnya di lambung dan esofagus, sakit kuning
(kulit menguning), dan kerusakan otak.
[12]
Efek pada organ di luar hati
Meskipun jarang, hepatitis C juga dapat berkaitan dengan Sindrom
Sjögren (kelainan autoimun), kadar trombosit darah yang rendah (di bawah
normal), penyakit kulit kronis, diabetes, dan limfoma non-Hodgkin.
[14]
Penyebab
Virus hepatitis C merupakan virus RNA yang berukuran kecil, bersampul, berantai tunggal, dengan sense positif.
[3] Virus ini merupakan anggota genus
hepacivirus dalam famili
Flaviviridae.
[9] Terdapat tujuh genotipe utama HCV.
[15]
Di Amerika Serikat, genotipe 1 merupakan penyebab pada 70% kasus
hepatitis, genotipe 2 pada 20%, dan genotipe lainnya masing-masing 1%.
[5] Genotipe 1 juga merupakan genotipe yang paling banyak ditemui di Amerika Selatan dan Eropa.
[3]
Penularan
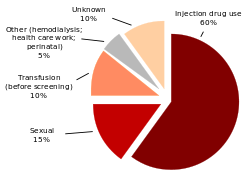
Hepatitis C infection in the United States by source
Metode utama penularan di negara maju adalah melalui penggunaan
narkoba suntik (IDU). Di negara berkembang metode penularan utamanya
adalah melalui transfusi darah dan prosedur medis yang tidak aman
[16] Penyebab penularan ini belum diketahui pada 20% kasus;
[17] namun banyak di antara kasus-kasus ini yang kemungkinan besar disebabkan oleh IDU.
[6]
Penggunaan narkoba suntik
Penggunaan narkoba suntik merupakan faktor risiko utama penularan virus hepatitis C di banyak negara di dunia.
[18]
Kajian di 77 negara menunjukkan bahwa 25 negara memiliki angka
hepatitis C pada populasi pengguna narkoba suntik antara 60% dan 80%,
termasuk di Amerika Serikat
[7] dan Cina.
[18] Di dua belas negara angkanya lebih besar dari 80%.
[7]
Sebanyak sepuluh juta pengguna narkoba suntik terinfeksi hepatitis C;
Cina (1,6 juta), Amerika Serikat (1,5 juta), dan Rusia (1,3 juta)
memiliki total terbanyak.
[7]
Angka hepatitis C pada warga binaan di lembaga pemasyarakatan di
Amerika Serikat sepuluh hingga dua puluh kali lipat dibandingkan dengan
populasi umum, dan penelitian ini mengaitkannya dengan perilaku berisiko
seperti penggunaan narkoba suntik dan pembuatan tato dengan peralatan
yang tidak steril.
[19][20]
Pajanan terkait layanan kesehatan
Transfusi darah, produk darah, dan transplantasi organ tanpa penapisan HCV menimbulkan risiko yang tinggi terkena infeksi.
[5]
Amerika Serikat mewajibkan penapisan universal pada 1992. Sejak saat
itu angka infeksi menurun dari sebelumnya satu dari 200 unit darah,
[21] menjadi hanya satu dari 10.000, hingga satu dari 10.000.000 unit darah
[6][17].
Risiko rendah tetap ada karena terdapat periode sekitar 11-70 hari
antara seorang pendonor darah yang kemungkinan menderita hepatitis C dan
hasil pemeriksaan darah yang positif.
[17] Beberapa negara belum melakukan penapisan hepatitis C karena masalah biaya.
[11]
Orang yang tertusuk jarum suntik bekas pakai penderita HCV memiliki peluang 1,8% untuk tertular penyakit hepatitis C.
[5] Risiko tersebut menjadi lebih tinggi jika jarum yang digunakan berlubang dan luka tusuk tersebut dalam.
[11]
Terdapat risiko paparan mukus ke darah; namun risiko tersebut rendah,
dan tidak ada risiko jika pajanan darah tersebut terjadi pada kulit yang
utuh.
[11]
Peralatan rumah sakit juga dapat menularkan hepatitis C termasuk:
penggunaan ulang jarum suntik dan spuit, vial obat yang digunakan
berkali-kali, kantong infus, dan peralatan bedah yang tidak steril.
[11]
Standar yang buruk di fasilitas pelayanan kesehatan umum dan gigi
menjadi penyebab utama penularan HCV di Mesir, negara dengan angka
infeksi tertinggi di dunia.
[22]
Hubungan seksual
Tidak diketahui apakah hepatitis C dapat ditularkan melalui hubungan seksual.
[23]
Meskipun terdapat hubungan antara aktivitas seksual berisiko tinggi dan
hepatitis C, belum jelas apakah penularan penyakit tersebut disebabkan
oleh penggunaan narkoba yang tidak dikatakan oleh pasien atau disebabkan
oleh seks itu sendiri.
[5]
Bukti yang ada mendukung bahwa tidak ada risiko pada pasangan
heteroseksual yang tidak berhubungan seks dengan orang lain selain
pasangan mereka.
[23]
Aktivitas seksual yang melibatkan trauma berat pada tepi bagian dalam
saluran anus, seperti penetrasi anus, atau yang terjadi ketika terdapat
infeksi menular seksual, termasuk HIV atau ulkud genital, cukup
berisiko.
[23]
Pemerintah Amerika Serikat merekomendasikan penggunaan kondom hanya
untuk mencegah penularan hepatitis C pada orang yang bergonta-ganti
pasangan.
[24]
Tindik di bagian tubuh
Tato juga dapat meningkatkan risiko penularan hepatitis C hingga dua atau tiga kali lipat.
[25] Ini bisa disebabkan karena peralatan yang tidak steril atau karena tinta yang digunakan terkontaminasi virus.
[25]
Tato atau tindik badan yang dilakukan sebelum pertengahan tahun 1980an
atau yang dilakukan secara tidak profesional menjadi salah satu
penyebabnya, karena masih buruknya teknik steril dalam kondisi tersebut.
Risiko tersebut semakin meningkat jika tato yang dibuat lebih besar.
[25] Hampir setengah dari warga binaan di lapas menggunakan peralatan pembuatan tato secara bersama-sama.
[25] Tato yang dibuat di tempat pembuatan tato yang sah jarang dikaitkan dengan infeksi HCV.
[26]
Kontak dengan darah
Benda perawatan pribadi seperti pisau cukur, sikat gigi, dan
peralatan manikur atau pedikur dapat berkontak dengan darah. Penggunaan
peralatan pribadi bersama-sama dengan orang lain berisiko menularkan
HCV.
[27][28] Orang-orang harus waspada terhadap luka iris dan luka terbuka atau perdarahan lain.
[28]
HCV tidak menular melalui kontak biasa, seperti berpelukan, berciuman,
atau penggunaan bersama peralatan makan atau peralatan memasak.
[28]
Penularan dari ibu ke anak
Penularan hepatitis C dari ibu yang terinfeksi ke anaknya terjadi pada kurang dari 10% kehamilan.
[29] Tidak ada tindakan yang dapat mencegah risiko ini.
[29] Penularan dapat terjadi selama kehamilan dan saat persalinan.
[17] Persalinan yang berlangsung lama dikaitkan dengan semakin tingginya risiko penularan.
[11]
Tidak ada bukti bahwa pemberian ASI menularkan HCV; namun, ibu yang
terinfeksi harus menghindari pemberian ASI jika puting ibu mengalami
pecah-pecah dan berdarah,
[30] atau jumlah virus dalam tubuhnya banyak.
[17]
Diagnosis
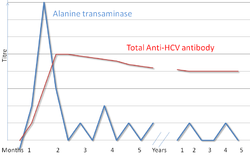
Profil serologi infeksi Hepatitis C
Tes diagnosis untuk hepatitis C termasuk: antibodi HCV, ELISA, Western blot, dan RNA HCV kuantitatif.
[5]
Polymerase chain reaction (PCR) dapat mendeteksi RNA HCV satu hingga
dua minggu setelah infeksi, sedangkan antibodi baru terbentuk dan baru
dapat ditemukan dalam waktu yang lebih lama.
[12]
Hepatitis C kronis merupakan infeksi dengan virus hepatitis C yang
menetap selama lebih dari enam bulan berdasarkan keberadaan RNA-nya.
[8] Karena infeksi kronis umumnya baru menunjukkan gejala setelah berpuluh tahun,
[8]
dokter biasanya baru menemukan kasus pada saat pemeriksaan fungsi hati
atau saat melakukan penapisan rutin pada orang berisiko tinggi.
Pemeriksaan ini tidak dapat membedakan antara infeksi akut dan infeksi
kronis.
[11]
Pemeriksaan darah
Pemeriksaan hepatitis C biasanya dimulai dengan pemeriksaan darah
untuk mendeteksi apakah ada antibodi terhadap HCV dengan menggunakan uji
imunoasai enzim (enzyme immunoassay).
[5]
Jika hasil pemeriksaan ini positif, dilakukan pemeriksaan kedua untuk
memastikan uji imunoasai dan untuk menentukan beratnya penyakit.
[5] Uji imunoblot rekombinan memastikan uji imunoasai tersebut, dan reaksi rantai polimerase RNA HCV menentukan beratnya.
[5]
Jika tidak ada RNA dan hasil imunoblot positif, orang tersebut pernah
mengalami infeksi namun sudah teratasi baik dengan pengobatan maupun
secara spontan; jika imunoblot negatif, artinya uji imunoasai salah.
[5] Uji imunoasai baru akan memberikan hasil positif enam hingga delapan minggu setelah infeksi.
[9]
Enzim hati dapat bervariasi selama tahap awal infeksi;
[8] rata-rata enzim tersebut mulai meningkat tujuh minggu setelah infeksi.
[9] Enzim hati tidak terlalu berkaitan dengan beratnya penyakit.
[9]
Biopsi
Biopsi hati dapat menentukan derajat kerusakan hati, namun prosedur tersebut memiliki beberapa risiko.
[3]
Perubahan khas yang biasanya terdeteksi melalui biopsi meliputi
limfosit di dalam jaringan hati, folikel limfoid di dalam trias
hepatika, dan perubahan pada saluran empedu.
[3] Terdapat beberapa pemeriksaan darah untuk menentukan tingkat kerusakan dan menyingkirkan perlunya biopsi.
[3]
Penapisan
Hanya 5–50% dari orang-orang yang terinfeksi di Amerika Serikat dan Kanada yang mengetahui status mereka.
[25] Pemeriksaan hepatitis C sangat dianjurkan untuk orang berisiko tinggi, termasuk orang yang memiliki tato.
[25]
Penapisan juga disarankan pada orang dengan peningkatan kadar enzim
hati, karena seringkali hal ini merupakan satu-satunya tanda hepatitis
kronis.
[31] Penapisan rutin tidak disarankan di Amerika Serikat.
[5]
Pencegahan
Hingga tahun 2011, belum ada vaksin untuk hepatitis C. Vaksin sedang
dikembangkan dan sebagian menunjukkan hasil yang menjanjikan.
[32]
Kombinasi strategi pencegahan, seperti program pertukaran jarum suntik
dan pengobatan untuk penyalahgunaan zat terlarang, menurunkan risiko
hepatitis C hingga 75% pada pengguna narkoba suntik.
[33]
Penapisan pada pendonor darah penting dilakukan pada tingkat nasional,
sesuai dengan universal precautions (pencegahan universal) di fasilitas
layanan kesehatan.
[9]
Di negara-negara yang tidak memiliki pasokan spuit steril yang cukup,
penyedia layanan kesehatan sebaiknya memberikan obat oral dibandingkan
dengan obat suntik.
[11]
Tata laksana
HCV menyebabkan infeksi kronis pada 50–80% orang yang terinfeksi.
Sekitar 40-80% dari kasus ini dapat dibersihkan dengan pengobatan.
[34][35] Pada kasus yang jarang, infeksi dapat bersih tanpa pengobatan.
[6] Orang yang menderita hepatitis C kronis harus menghindari alkohol dan obat-obat yang dapat merusak hati,
[5] dan harus mendapat vaksinasi untuk hepatitis A dan hepatitis B.
[5] Orang yang mengalami sirosis harus menjalani pemeriksaan ultrasonografi untuk mendeteksi kanker hati.
[5]
Obat-obatan
Orang yang terbukti mengalami kelainan hati karena infeksi HCV harus berobat.
[5]
Pengobatan saat ini menggunakan kombinasi interferon pegilasi dan obat
antivirus ribavirin selama 24 atau 48 minggu, bergantung pada tipe HCV.
[5] Hasilnya lebih baik pada 50–60% pasien yang diobati.
[5]
Kombinasi boceprevir atau telaprevir dengan ribavirin dan peginterferon
alfa meningkatkan respons antivirus terhadap hepatitis C genotipe 1.
[36][37][38]
Efek samping pengobatan sering terjadi; setengah dari pasien yang
diobati terserang gejala yang mirip flu, dan sepertiga dari mereka
mengalami masalah emosional.
[5]
Pengobatan yang dilakukan dalam enam bulan pertama akan lebih efektif
daripada pengobatan yang dilakukan setelah hepatitis C menjadi kronis.
[12]
Jika seseorang mengalami infeksi baru dan virus belum dapat dihilangkan
setelah delapan hingga dua belas minggu, pasien tersebut sebaiknya
menjalani pengobatan interferon pegilasi selama 24 minggu.
[12]
Bagi pasien dengan thalasemia (kelainan darah), ribavirin sepertinya
dapat digunakan, namun meningkatkan kebutuhan akan transfusi.
[39]
Para ahli yang mendukung mengklaim terapi alternatif sebagai terapi
yang bermanfaat pada hepatitis C termasuk milk thistle (silybum),
ginseng, dan colloidal silver/perak koloid.
[40]
Namun, belum ada terapi alternatif yang terbukti memberikan hasil yang
lebih baik pada hepatitis C, dan tidak ada bukti bahwa terapi alternatif
memberikan efek sedikitpun pada virus.
[40][41][42]
Prognosis
Respons terhadap pengobatan berbeda-beda berdasarkan genotipenya.
Respons berlanjut terjadi pada kira-kira 40-50% orang dengan HCV
genotipe 1 yang menjalani pengobatan selama 48 minggu.
[3] Respons berlanjut terjadi pada 70-80% dari pasien dengan HCV genotipe 2 dan 3 yang menjalani pengobatan selama 24 minggu.
[3]
Respon berlanjut terdapat pada kira-kira 65% dari pasien dengan
genotipe 4 yang menjalani pengobatan selama 48 minggu. Bukti pengobatan
pada penyakit dengan genotipe 6 masih sangat sedikit saat ini, dan bukti
yang ada adalah pengobatan selama 48 minggu dengan dosis yang sama
seperti dosis yang diberikan kepada pasien penyakit genotipe 1.
[43]
Epidemiologi

Prevalensi hepatitis C di seluruh dunia tahun 1999
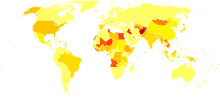
Disability-adjusted life year untuk hepatitis C pada 2004 per 100.000 penduduk
|
██ no data ██ <10 ██ 10-15 ██ 15-20 ██ 20-25 ██ 25-30 ██ 30-35
|
██ 35-40 ██ 40-45 ██ 45-50 ██ 50-75 ██ 75–100 ██ >100
|
Antara 130 dan 170 juta jiwa, atau ~3% dari populasi dunia, hidup dengan hepatitis C kronis.
[44]
Sekitar 3–4 juta orang terinfeksi setiap tahunnya, dan lebih dari
350.000 orang meninggal setiap tahun akibat penyakit yang berkaitan
dengan hepatitis C.
[44]
Angka tersebut meningkat tinggi pada abad ke-20 akibat kombinasi
pengguna narkoba suntik dan pemberian obat suntik atau peralatan medis
yang tidak disterilkan.
[11]
Di Amerika Serikat, sekitar 2% penduduk menderita hepatitis C,
[5]
dengan 35.000 hingga 185.000 kasus baru per tahun. Angka tersebut telah
menurun di negara Barat sejak 1990-an karena penapisan darah semakin
ketat sebelum transfusi.
[12]
Angka kematian per tahun akibat HCV di Amerika Serikat berkisar 8.000
hingga 10.000. Kemungkinan angka mortalitas tersebut masih akan
meningkat, karena sakit atau meninggalnya orang yang terinfeksi melalui
transfusi sebelum masa pemeriksaan HCV.
[45]
Angka infeksi lebih tinggi di beberapa negara di Afrika dan Asia.
[46] Negara dengan angka infeksi yang sangat tinggi meliputi Mesir (22%), Pakistan (4,8%) dan Cina (3,2%).
[44]
Angka yang tinggi di Mesir dikaitkan dengan kampanye pengobatan massal
untuk schistosomiasis yang sekarang dihentikan, menggunakan spuit kaca
yang tidak disterilisasi dengan benar.
[11]
Sejarah
Pada pertengahan 1970-an, Harvey J. Alter, Kepala Bagian Penyakit
Menular di Departemen Kedokteran Transfusi di National Institutes of
Health, dan tim penelitiannya menunjukkan bahwa sebagian besar kasus
hepatitis pasca-transfusi darah tidak disebabkan oleh virus hepatitis A
maupun B. Meski terdapat temuan ini, usaha penelitian yang dilakukan
pada tingkat internasional untuk mengidentifikasi virus gagal selama
dekade berikutnya. Pada tahun 1987, Michael Houghton, Qui-Lim Choo, dan
George Kuo di Chiron Corporation, berkolaborasi dengan Dr. D.W. Bradley
dari Centers for Disease Control and Prevention, menggunakan pendekatan
kloning molekuler baru untuk mengidentifikasi organisme asing dan
mengembangkan suatu uji diagnostik.
[47]
Pada 1988, Alter mengonfirmasi virus tersebut dengan memverifikasi
keberadaannya di sebuah panel spesimen hepatitis non A dan non B. Pada
April 1989, penemuan HCV dipublikasikan dalam dua artikel di jurnal
Science.
[48][49] Penemuan tersebut membawa kemajuan berarti dalam hal diagnosis dan pengobatan antivirus yang lebih baik.
[47]
Pada tahun 2000, Drs. Alter dan Houghton diberi penghargaan yakni
Lasker Award for Clinical Medical Research karena telah "merintis karya
yang membawa ke penemuan virus yang menyebabkan hepatitis C dan
pengembangan metode penapisan sehingga telah menurunkan risiko hepatitis
terkait transfusi darah di AS dari 30% pada 1970 menjadi hingga hampir
nol pada 2000."
[50]
Chiron mendaftarkan beberapa paten virus dan diagnosisnya.
[51]
Aplikasi paten pesaingnya dari CDC dibatalkan pada 1990 setelah Chiron
membayar $1,9 juta kepada CDC dan $337.500 kepada Bradley. Pada 1994,
Bradley menuntut Chiron, berusaha membatalkan validasi paten, berhasil
membuat dirinya diakui sebagai rekan penemu (ko-inventor), dan
mendapatkan kerugian dan pendapatan dari royalti. Dia membatalkan
tuntutannya pada 1998 setelah kalah sebelum sidang banding.
[52]
Masyarakat dan budaya
The World Hepatitis Alliance mengadakan Hari Hepatitis Sedunia, yang diselenggarakan setiap tahun pada tanggal 28 Juli.
[53]
Biaya pengobatan hepatitis C cukup bermakna baik terhadap pribadi
maupun masyarakat. Di Amerika Serikat rata-rata biaya kesehatan seumur
hidup untuk penyakit ini diperkirakan 33.407 dolar AS pada tahun 2003,
[54] dengan biaya transplantasi hati kira-kira 200.000 dolar AS pada 2011.
[55] Di Kanada biaya satu kali pengobatan antivirus mencapai 30.000 dolar Kanada pada 2003,
[56] sedangkan di Amerika Serikat biaya tersebut berkisar antara 9.200 dan 17.600 pada dollar AS 1998.
[54]
Di banyak wilayah di dunia banyak orang yang tidak mampu membayar obat
antivirus karena mereka tidak memiliki asuransi atau asuransi kesehatan
mereka tidak menanggung obat antivirus.
[57]
Penelitian
Sejak 2011, sekitar seratus obat sedang dikembangkan untuk hepatitis C.
[55] Obat-obatan ini termasuk vaksin untuk hepatitis, imunomodulator, dan penghambat cyclophilin.
[58] Pengobatan baru yang menjanjikan ini telah terwujud karena pemahaman yang lebih baik mengenai virus hepatitis C.
[59]
Referensi
- ^ a b Ryan KJ, Ray CG (editors), ed (2004). Sherris Medical Microbiology (edisi ke-4th). McGraw Hill. hlm. 551–2. ISBN 0838585299.
- ^ Houghton M (November 2009). "The long and winding road leading to the identification of the hepatitis C virus". Journal of Hepatology 51 (5): 939–48. doi:10.1016/j.jhep.2009.08.004. PMID 19781804.
- ^ a b c d e f g h i j k Rosen, HR (2011-06-23). "Clinical practice. Chronic hepatitis C infection.". The New England journal of medicine 364 (25): 2429–38. PMID 21696309.
- ^ Maheshwari, A (2008-07-26). "Acute hepatitis C.". Lancet 372 (9635): 321–32. doi:10.1016/S0140-6736(08)61116-2. PMID 18657711.
- ^ a b c d e f g h i j k l m n o p q r s t u v Wilkins, T (2010-06-01). "Hepatitis C: diagnosis and treatment.". American family physician 81 (11): 1351–7. PMID 20521755.
- ^ a b c d e Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future.. Springer Verlag. 6 November 2011. hlm. 4. ISBN 9781461411918.
- ^ a b c d Nelson,
PK (2011-08-13). "Global epidemiology of hepatitis B and hepatitis C in
people who inject drugs: results of systematic reviews.". Lancet 378 (9791): 571–83. doi:10.1016/S0140-6736(11)61097-0. PMID 21802134.
- ^ a b c d Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future.. Springer Verlag. 6 November 2011. hlm. 103–104. ISBN 9781461411918.
- ^ a b c d e f Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael (2010). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (edisi ke-7th ed.). Philadelphia, PA: Churchill Livingstone/Elsevier. hlm. Chapter 154. ISBN 978-0443068393.
- ^ Mueller, S (2009-07-28). "Alcoholic liver disease and hepatitis C: a frequently underestimated combination.". World journal of gastroenterology : WJG 15 (28): 3462–71. PMID 19630099.
- ^ a b c d e f g h i j Alter, MJ (2007-05-07). "Epidemiology of hepatitis C virus infection.". World journal of gastroenterology : WJG 13 (17): 2436–41. PMID 17552026.
- ^ a b c d e Ozaras, R (2009 Apr). "Acute hepatitis C: prevention and treatment.". Expert review of anti-infective therapy 7 (3): 351–61. PMID 19344247.
- ^ Louie, KS (2011 Jan). "Prevalence of thrombocytopenia among patients with chronic hepatitis C: a systematic review.". Journal of viral hepatitis 18 (1): 1–7. PMID 20796208.
- ^ Nakano
T, Lau GM, Lau GM, Sugiyama M, Mizokami M (December 2011). "An updated
analysis of hepatitis C virus genotypes and subtypes based on the
complete coding region". Liver Int.. doi:10.1111/j.1478-3231.2011.02684.x. PMID 22142261.
- ^ Maheshwari, A (2010 Feb). "Management of acute hepatitis C.". Clinics in liver disease 14 (1): 169–76; x. PMID 20123448.
- ^ a b c d e Pondé, RA (2011 Feb). "Hidden hazards of HCV transmission.". Medical microbiology and immunology 200 (1): 7–11. PMID 20461405.
- ^ a b Xia, X (2008 Oct). "Epidemiology of HCV infection among injection drug users in China: systematic review and meta-analysis.". Public health 122 (10): 990–1003. doi:10.1016/j.puhe.2008.01.014. PMID 18486955.
- ^ Imperial, JC (2010 Jun). "Chronic hepatitis C in the state prison system: insights into the problems and possible solutions.". Expert review of gastroenterology & hepatology 4 (3): 355–64. PMID 20528122.
- ^ Vescio, MF (2008 Apr). "Correlates of hepatitis C virus seropositivity in prison inmates: a meta-analysis.". Journal of epidemiology and community health 62 (4): 305–13. PMID 18339822.
- ^ Marx, John (2010). Rosen's emergency medicine: concepts and clinical practice 7th edition. Philadelphia, PA: Mosby/Elsevier. hlm. 1154. ISBN 9780323054720.
- ^ "Highest Rates of Hepatitis C Virus Transmission Found in Egypt". Al Bawaba. 9 Agustus 2010. Diakses pada 27 Agustus 2010.
- ^ a b c Tohme RA, Holmberg SD (June 2010). "Is sexual contact a major mode of hepatitis C virus transmission?". Hepatology 52 (4): 1497–505. doi:10.1002/hep.23808. PMID 20635398.
- ^ "Hepatitis C Group Education Class". United States Department of Veteran Affairs.
- ^ a b c d e f Jafari, S (2010 Nov). "Tattooing and the risk of transmission of hepatitis C: a systematic review and meta-analysis.". International journal of infectious diseases : IJID : official publication of the International Society for Infectious Diseases 14 (11): e928-40. PMID 20678951.
- ^ "Hepatitis C". Center for Disease Control and Prevention. Diakses pada 2 Januari 2012.
- ^ Lock G, Dirscherl M, Obermeier F, et al. (September 2006). "Hepatitis C —contamination of toothbrushes: myth or reality?". J. Viral Hepat. 13 (9): 571–3. doi:10.1111/j.1365-2893.2006.00735.x. PMID 16907842.
- ^ a b c "Hepatitis C". FAQ – CDC Viral Hepatitis. Diakses pada 2 Januari 2012.
- ^ a b Lam, NC (2010-11-15). "Caring for pregnant women and newborns with hepatitis B or C.". American family physician 82 (10): 1225–9. PMID 21121533.
- ^ Mast EE (2004). "Mother-to-infant hepatitis C virus transmission and breastfeeding". Advances in Experimental Medicine and Biology 554: 211–6. PMID 15384578.
- ^ Senadhi, V (2011 Jul). "A paradigm shift in the outpatient approach to liver function tests.". Southern medical journal 104 (7): 521–5. PMID 21886053.
- ^ Halliday, J (2011 May). "Vaccination for hepatitis C virus: closing in on an evasive target.". Expert review of vaccines 10 (5): 659–72. doi:10.1586/erv.11.55. PMID 21604986.
- ^ Hagan,
H (2011-07-01). "A systematic review and meta-analysis of interventions
to prevent hepatitis C virus infection in people who inject drugs.". The Journal of infectious diseases 204 (1): 74–83. PMID 21628661.
- ^ Torresi, J (2011 Jun). "Progress in the development of preventive and therapeutic vaccines for hepatitis C virus.". Journal of hepatology 54 (6): 1273–85. doi:10.1016/j.jhep.2010.09.040. PMID 21236312.
- ^ Ilyas, JA (2011 Aug). "An overview of emerging therapies for the treatment of chronic hepatitis C.". Clinics in liver disease 15 (3): 515–36. PMID 21867934.
- ^ Foote
BS, Spooner LM, Belliveau PP (September 2011). "Boceprevir: a protease
inhibitor for the treatment of chronic hepatitis C". Ann Pharmacother 45 (9): 1085–93. doi:10.1345/aph.1P744. PMID 21828346.
- ^ Smith
LS, Nelson M, Naik S, Woten J (May 2011). "Telaprevir: an NS3/4A
protease inhibitor for the treatment of chronic hepatitis C". Ann Pharmacother 45 (5): 639–48. doi:10.1345/aph.1P430. PMID 21558488.
- ^ Ghany MG, Nelson DR, Strader DB, Thomas DL, Seeff LB (October 2011). "An
update on treatment of genotype 1 chronic hepatitis C virus infection:
2011 practice guideline by the American Association for the Study of
Liver Diseases". Hepatology 54 (4): 1433–44. doi:10.1002/hep.24641. PMID 21898493.
- ^ Alavian
SM, Tabatabaei SV (April 2010). "Treatment of chronic hepatitis C in
polytransfused thalassaemic patients: a meta-analysis". J. Viral Hepat. 17 (4): 236–44. doi:10.1111/j.1365-2893.2009.01170.x. PMID 19638104.
- ^ a b Hepatitis C and CAM: What the Science Says. NCCAM March 2011. (Retrieved 07 March 2011)
- ^ Liu,
J (2003 Mar). "Medicinal herbs for hepatitis C virus infection: a
Cochrane hepatobiliary systematic review of randomized trials.". The American journal of gastroenterology 98 (3): 538–44. PMID 12650784.
- ^ Rambaldi, A (2007-10-17). "Milk thistle for alcoholic and/or hepatitis B or C virus liver diseases.". Cochrane database of systematic reviews (Online) (4): CD003620. PMID 17943794.
- ^ Fung J, Lai CL, Hung I, et al. (September 2008). "Chronic hepatitis C virus genotype 6 infection: response to pegylated interferon and ribavirin". The Journal of Infectious Diseases 198 (6): 808–12. doi:10.1086/591252. PMID 18657036.
- ^ a b c "WHO Hepatitis C factsheet". 6 November 2011. Diakses pada 13 Juli 2011.
- ^ Colacino, ed. by J. M. (2004). Hepatitis prevention and treatment. Basel: Birkhäuser. hlm. 32. ISBN 9783764359560.
- ^ al.], edited by Gary W. Brunette ... [et. CDC health information for international travel : the Yellow Book 2012. New York: Oxford University. hlm. 231. ISBN 9780199769018.
- ^ a b Boyer, JL (2001). Liver cirrhosis and its development: proceedings of the Falk Symposium 115. Springer. hlm. 344. ISBN 9780792387602.
- ^ Choo
QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (April 1989).
"Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral
hepatitis genome". Science 244 (4902): 359–62. doi:10.1126/science.2523562. PMID 2523562.
- ^ Kuo G, Choo QL, Alter HJ, et al. (April 1989). "An assay for circulating antibodies to a major etiologic virus of human non-A, non-B hepatitis". Science 244 (4902): 362–4. doi:10.1126/science.2496467. PMID 2496467.
- ^ Winners Albert Lasker Award for Clinical Medical Research, The Lasker Foundation. Retrieved 20 February 2008.
- ^ Houghton, M., Q.-L. Choo, and G. Kuo. NANBV Diagnostics and Vaccines. European Patent No. EP-0-3 18-216-A1. European Patent Office (filed 18 November 1988, published 31 May 1989).
- ^ Wilken, Judge. "United States Court of Appeals for the Federal Circuit". United States Court of Appeals for the Federal Circuit. Diakses pada 11 Januari 2012.
- ^ Eurosurveillance editorial, team (2011-07-28). "World Hepatitis Day 2011.". Euro surveillance : bulletin europeen sur les maladies transmissibles = European communicable disease bulletin 16 (30). PMID 21813077.
- ^ a b Wong, JB (2006). "Hepatitis C: cost of illness and considerations for the economic evaluation of antiviral therapies.". PharmacoEconomics 24 (7): 661–72. PMID 16802842.
- ^ a b El Khoury, A. C. (1 December 2011). "Economic burden of hepatitis C-associated diseases in the United States". Journal of Viral Hepatitis. doi:10.1111/j.1365-2893.2011.01563.x.
- ^ "Hepatitis C Prevention, Support and Research ProgramHealth Canada". Public Health Agency of Canada. 1 November 2003. Diakses pada 10 Januari 2012.
- ^ Zuckerman, edited by Howard Thomas, Stanley Lemon, Arie (2008). Viral Hepatitis. (edisi ke-3rd ed.). Oxford: John Wiley & Sons. hlm. 532. ISBN 9781405143882.
- ^ Ahn, J (2011 Aug). "Hepatitis C therapy: other players in the game". Clinics in liver disease 15 (3): 641–56. doi:10.1016/j.cld.2011.05.008. PMID 21867942.
- ^ Vermehren, J (2011 Feb). "New HCV therapies on the horizon.". Clinical
microbiology and infection : the official publication of the European
Society of Clinical Microbiology and Infectious Diseases 17 (2): 122–34. PMID 21087349.